肥胖是一种脂肪过量沉积引起的慢性复杂疾病。肥胖会增加患2型糖尿病和心脏病的风险,影响骨骼健康和生殖系统,并增加罹患癌症的风险。根据WHO的定义,成人BMI≥25时为超重,BMI≥30时为肥胖。据WHO统计,2022年有25亿成人(18 岁及以上)超重,其中8.9亿人为肥胖。
一、现有减肥药物
肥胖的初始治疗为饮食疗法、运动等,后续可以通过药物、手术等手段进行干预治疗。目前针对肥胖患者首选药物为GLP-1R激动剂,例如司美格鲁肽,替尔泊肽和利拉鲁肽。此类药物减重效果显著,Retatrutide在48周时即可减重22%。
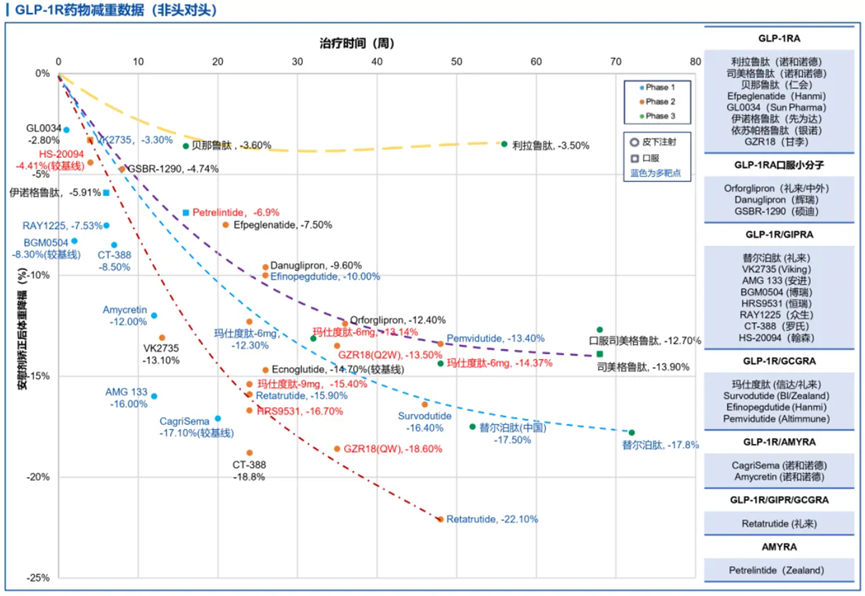
然而GLP-1R激动剂并不完美,存在以下问题。第一,耐受性差,用药超过1年的患者不足50%,不良反应发生率在89%左右。
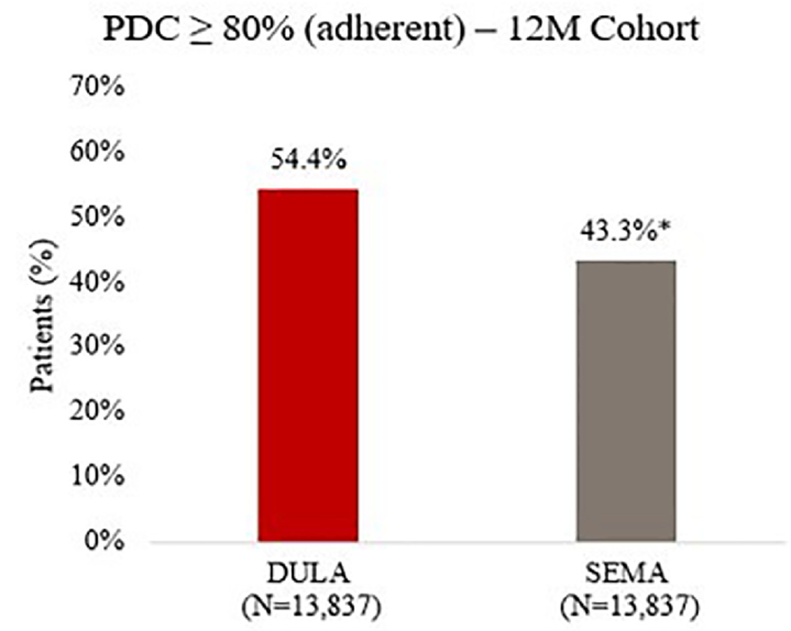
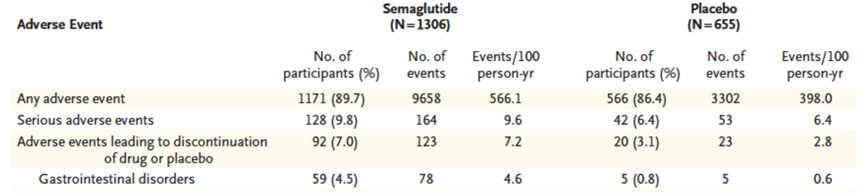
第二,减重过程肌肉流失,减掉的体重中三分之一为瘦体重(去脂体重)。
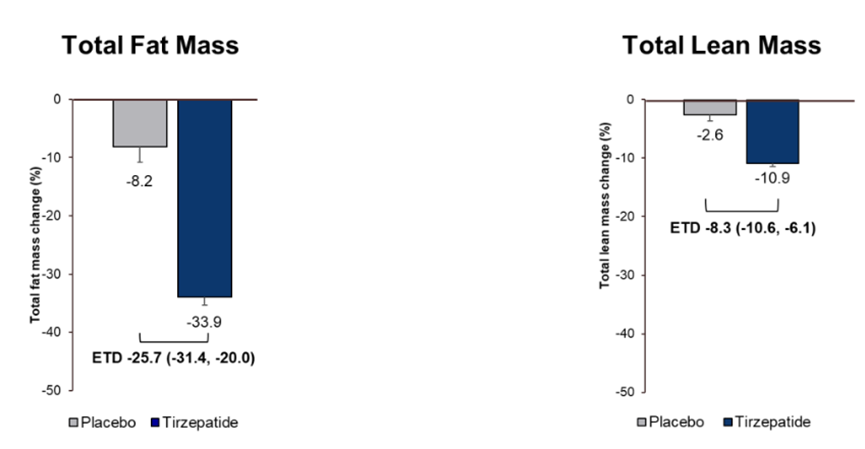
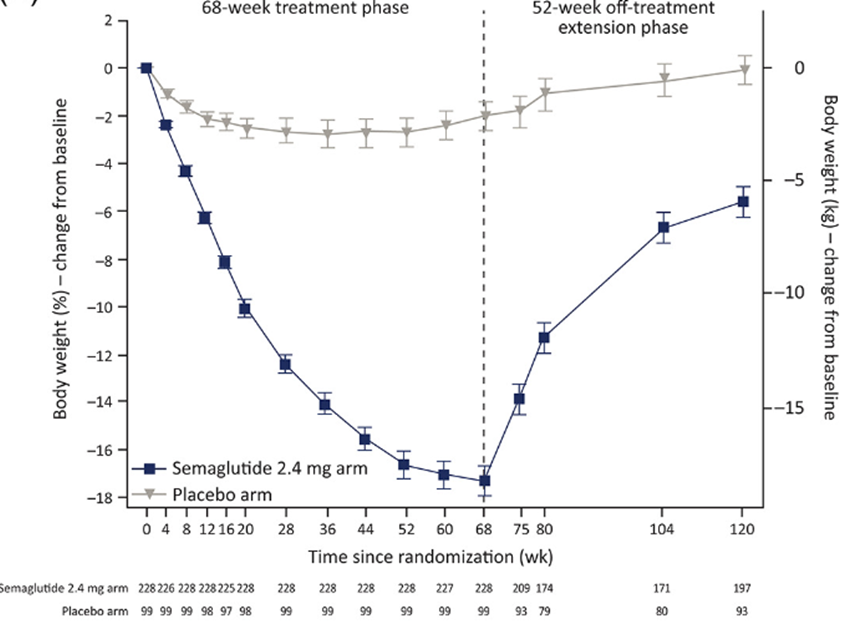
第三,停药后体重反弹严重,一年治疗后停药,平均恢复体重 11.6%。
为此业界寻找新靶点和新技术,解决GLP-1R激动剂不足。siRNA是近年热门的技术,基于碱基配对的原理,催化靶向mRNA的降解,通过递送手段实现长效干预。作为一种高效、长效和高成功率的技术,siRNA自2019年起开始被应用于减肥药领域。
二、siRNA减肥药研究之旅
1.TGF-β/cox-2
TGF-β/cox-2 siRNA 用于治疗肥胖起源于临床试验中的意外发现。
2020年10月,在STP705治疗isSCC临床IIa期试验中,高剂量组120µg受试者的病灶组织样本显示,皮下脂肪层变窄,可见脂肪组织坏死,提示STP705可能用于治疗肥胖。后续圣诺开展了临床前小猪模型POC,持续3周每周一次输注STP705,平均皮下厚度可明显减少。
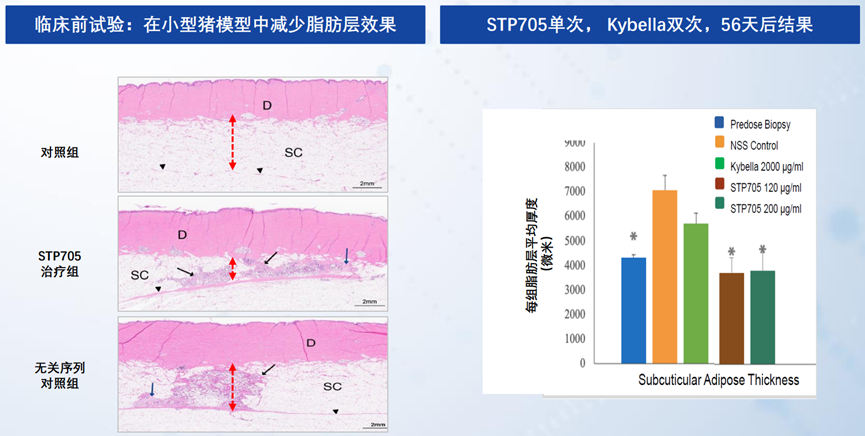
2022年8月,圣诺启动1期临床,评估接受腹部整形术的成年受试者皮下注射STP705的安全性和耐受性。
研究方案包括3个治疗周期,间隔28天给药。每个治疗周期需要进行7次皮下注射,包括0.5ml及1.0ml剂量(每次注射)的STP705 120 μg、240 μg或360 μg以及1.0ml的安慰剂。患者双盲随机分组并在下腹部7个1cm2的区域进行注射。8名年龄在18至65岁的受试者接受了注射,并在手术后2天和7天进行了随访。从最后一轮注射后28天获得的全腹部去脂术切除标本中,采集了来自7个注射部位的组织样本,并在整个研究过程中进行安全性评估(包括LSR评估),且收集了全部的不良事件。通过对采集的组织样本进行盲法组织学分析来评估STP705的溶脂和炎症效应,并根据观察到的炎症反应程度对每个样本进行组织学评分。
2023年11月,圣诺在新闻稿中公开临床结果,STP705在所有剂量、浓度和体积下均具有良好的耐受性,极少出现局部皮肤反应(LSR),240 μg/1ml剂量下药效最佳。圣诺计划在2024年开启STP705 II期临床。
2.INHBE
2022年7月,Alnylam公司在Nature Communications发表研究,揭示抑制INHBE可用于治疗腹部肥胖。研究人员通过英国Biobank中36万人的外显子组序列,识别与WHRadjBMI(BMI调整后腰臀比)相关的基因。WHRadjBMI是一种腹部脂肪替代指标,并且与冠心病和2型糖尿病有关。研究结果表明,INHBE pLOF(预测功能丧失)变异与较低的 WHRadjBMI 相关。INHBE主要在肝脏中表达,编码抑制素 βE 亚基。体外研究显示,INHBE pLOF变异会导致分泌蛋白水平降低90%。INHBE pLOF 携带者具有良好的代谢特征,包括甘油三酯降低、HDL-C增加和空腹血糖降低。
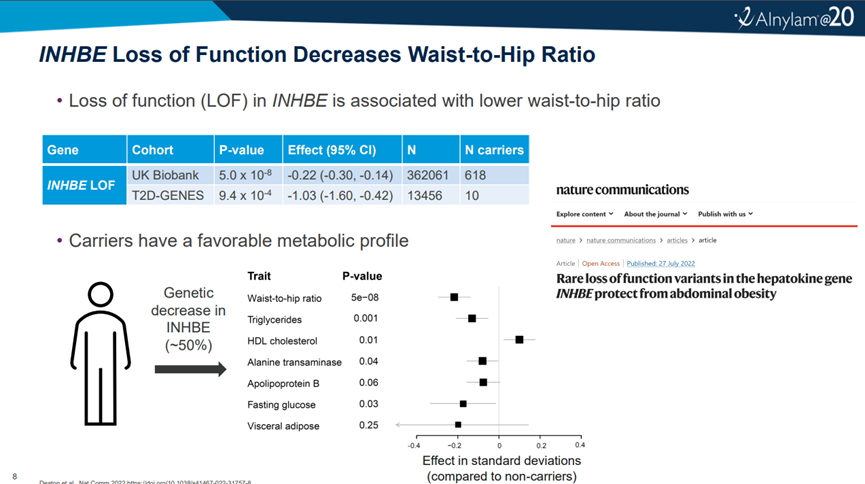
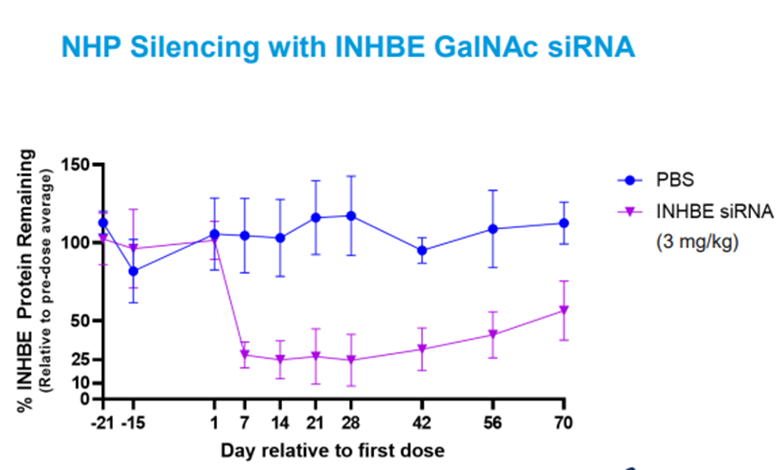
2022年12月,Alnylam在研发日上正式披露INHBE研发项目。2023年12月,Alnylam在研发日上进一步披露了ALN-INHBE临床前研究数据,通过GalNAc siRNA在7天后能够显著降低NHP中INHBE蛋白水平。Alnylam计划在2024年确定INHBE候选化合物。
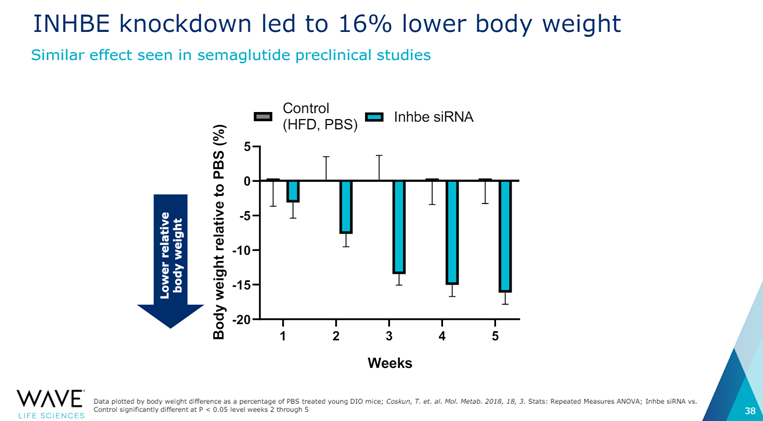
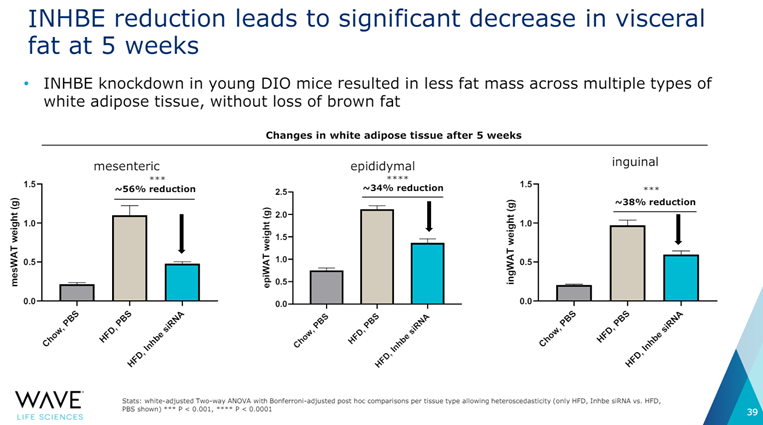
2023年9月,Wave公司在研发日披露了INHBE GalNAc siRNA项目。在小鼠模型上使用INHBE siRNA,5周内可以减轻16%体重, 显著减少内脏脂肪。Wave计划在2024年Q4确定候选化合物,2025年Q1启动临床试验。
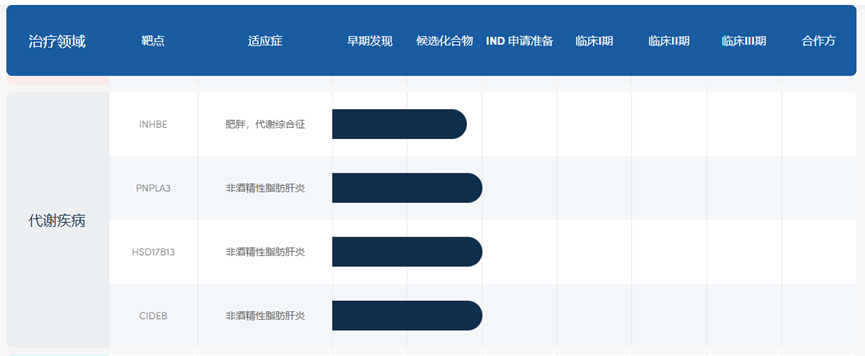
2024年1月,上海舶望在其网站上公开了INHBE siRNA项目,目前仍处于临床前研究阶段。
2024年2月,Arrowhead公司在一季度电话会上,披露了INHBE siRNA项目ARO-INHBE。在小鼠模型上使用siRNA沉默INHBE后,可以减轻20%以上的体重。目前Arrowhead已经确定候选化合物,计划在2024年底提交CTA。
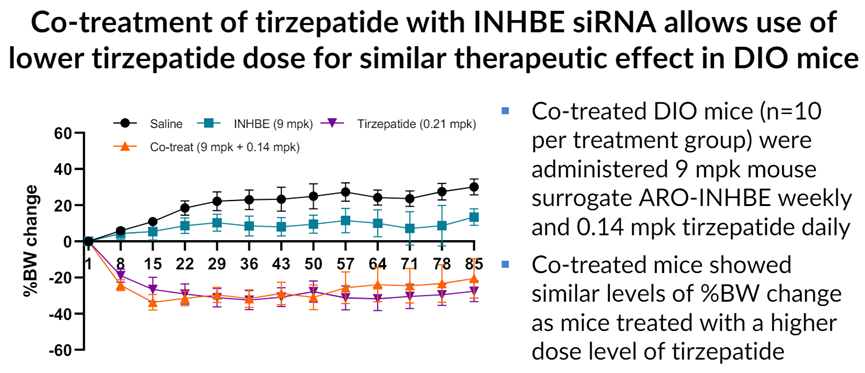
2024年6月,Arrowhead在ADA大会上披露了ARO-INHBE临床前数据。在DIO(饮食诱导肥胖)小鼠中,ARO-INHBE降低26%脂肪的同时,保持肌肉含量。
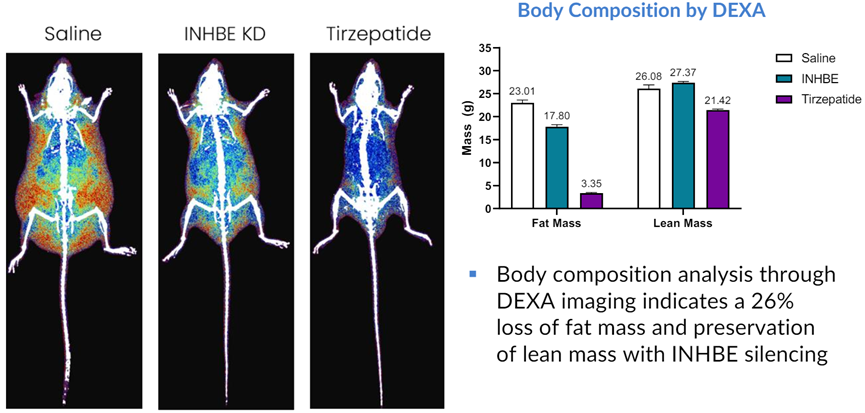
ARO-INHBED单药减重效果不及替尔泊肽,联合用药可降低替尔泊肽剂量。
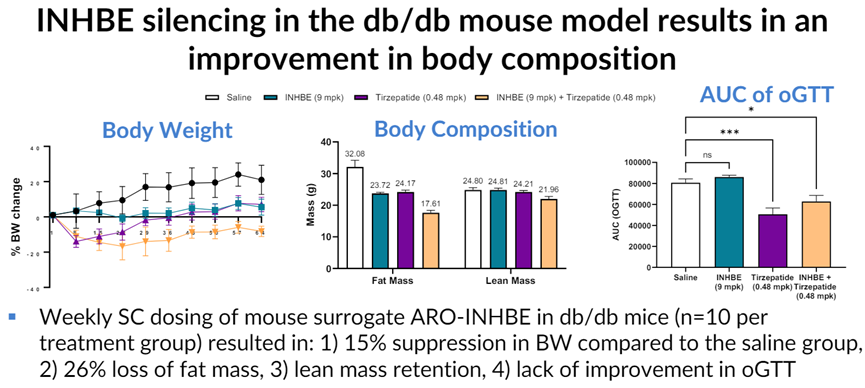
在db/db小鼠中,ARO-INHBE能够产生类似效果。
此外,再生元最早在2020年开始布局INHBE siRNA项目,但一直未有进展更新,考虑到再生元与Alnylam自2018年起已经深度合作多年,INHBE siRNA可能已交由Alnylam进行研发。
3.GPR75
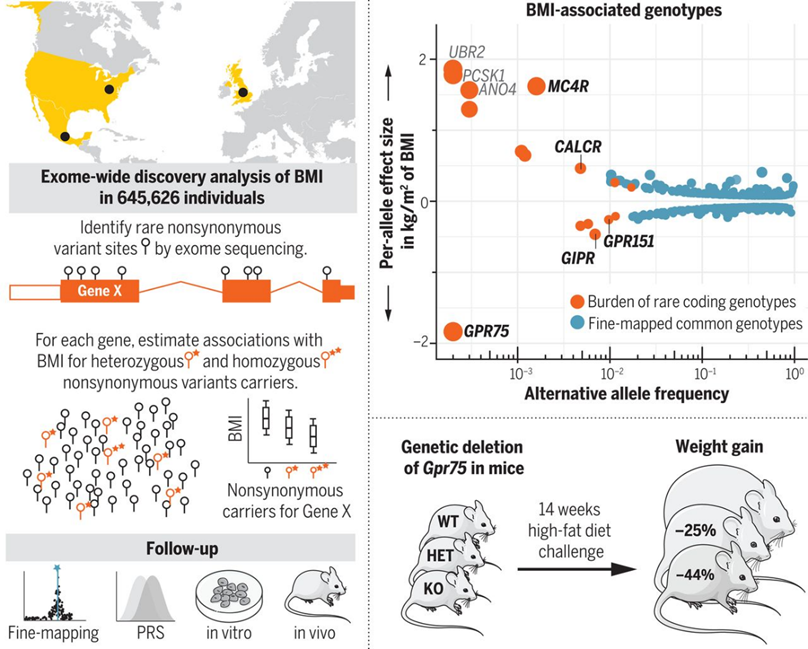
2021年7月,再生元在Science发表研究,通过对64 万人进行外显子测序,发现GPR75(G蛋白偶联受体75)基因拷贝突变杂合子个体的体重指数(BMI)较低,体重比没有突变的个体轻约 5.3 公斤,肥胖风险降低 54%,并显示出糖尿病相关参数的改善。在高脂饮食模型中,敲除GPR75 基因的小鼠能够抵抗高脂诱导体重增加(最高降低44%),并改善血糖水平。这些研究显示,抑制 GPR75 信号通路可能用于治疗为肥胖。
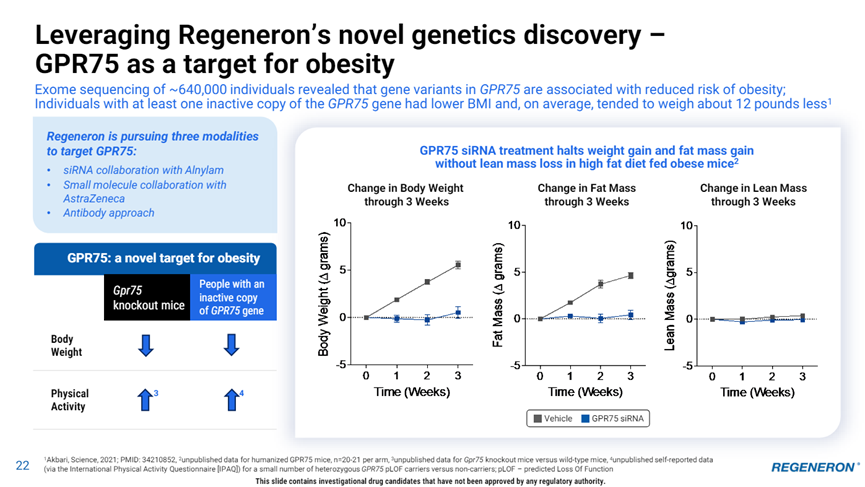
2024年1月,再生元在JP Morgan大会上,披露了GPR75siRNA体内试验数据,GPR75 siRNA可阻止高脂饮食的肥胖小鼠的体重和脂肪量增加,且无肌肉损失。
4.KHK
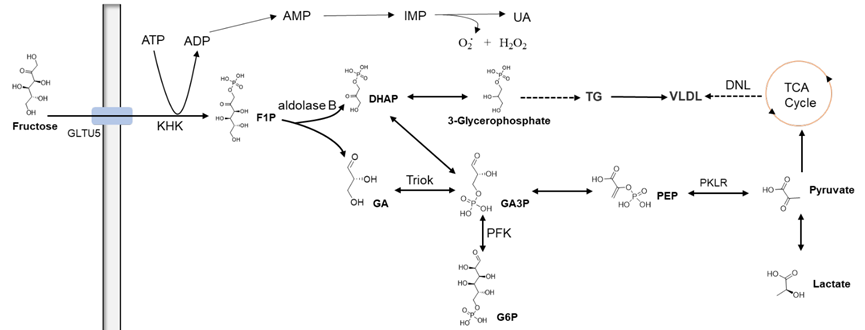
KHK,全称为己酮糖激酶,分为KHK-A和KHK-C,在果糖代谢中,可催化果糖生成果糖-1-磷酸(F1P),同时伴随着三磷酸腺苷(ATP)耗竭,ATP的消耗将导致活性氧(ROS)和尿酸(UA)的产生。F1P经aldolase B转换为DHAP和GA。GA被三糖激酶(Triok)磷酸化为GA3P, GA3P可以通过糖异生合成葡萄糖,此外GA3P还可以代谢成乳酸和丙酮酸,用于脂肪生成,显著提高新生脂质(DNL)的合成。
2020年12月,Alnylam首次在研发日上披露了KHK GalNAc siRNA药物ALN-KHK。
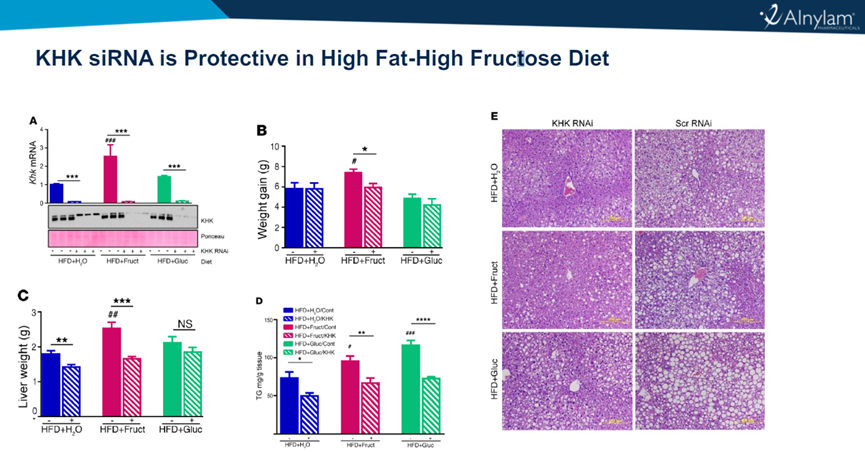
2023年3月,Alnylam启动1/2 期临床,评估 ALN-KHK对超重至肥胖健康志愿者和患有 2 型糖尿病的肥胖患者的作用。

2024年6月,Alnylam在ADA会议上公开了ALN-KHK中期结果。BMI 为 27-34.9 kg/m2的健康成年受试者按 3:1 的比例,随机接受单次皮下 ALN-KHK 或安慰剂治疗。在3个月内,评估了25、75、150、300 和 600 mg共5个剂量组,进行了9个月的随访。共有40名受试者入组(平均年龄为45.4岁,平均BMI 29.7kg/m 2;67.5%为男性)。数据截止,所有AE轻微可控。ALN-KHK 剂量增加与 FTT(果糖耐受测试) 后血清果糖曲线下面积 (AUC) 和尿液果糖分数的剂量和时间依赖性增加有关。初步数据显示,第85天服用300 mg时,血清果糖平均AUC(SD)从基线增加 178.0%(84.4%)。还观察到 FTT 后FGF21减少。
Alnylam计划在2024年启动ALN-KHK B部分研究。
5.其他靶点
此外还有一些冷门靶点,被用于研究减重,但以下药物仍处于临床前研究阶段。
药物 | 靶点 | 公司 | 披露时间 |
ASXL2 siRNA | ASXL2 | Altamira Therapeutics | 2023年5月 |
OLX702A | MARC1 | OliX Pharmaceuticals | 2023年6月 |
BF-114 | SPTBN1 | Bullfrogai | 2023年12月 |
三、未来展望
1.联用GLP-1
从INHBE、GPR75等靶点公开的临床前数据看,减重效果有限,但能够最大程度减去脂肪,保留肌肉。因此,未来可以与GLP-1药物协同使用。治疗初期,GLP-1 与INHBE/GPR75 siRNA联合使用快速减重。由于INHBE/GPR75 siRNA加入,可以一定程度减少GLP-1剂量,进而降低不良反应发生率,提高药物耐受性。后续单独INHBE/GPR75 siRNA,利用siRNA长效特点,维持脂肪分解,防止体重反弹。
2.医美局部减脂
根据Rabin Research Report 2019年的调查报告显示,不同身体部位减脂市场宽阔,仅美国潜治疗人群高达3200万。传统侵入性方式如吸脂手术,存在皮肤松弛,术后恢复期长等问题,因此非侵入性治疗手段越来越受欢迎。siRNA药物(例如STP705)可以通过局部注射的方式,减少特定身体部位脂肪,通过长效方式,持续发挥作用。

目前siRNA减肥药进展缓慢,研发进度最快的为Alnylam的ALN-KHK,刚刚完成1期临床,其余药物仍处于临床前研究阶,预计最快2029年首款siRNA减肥药上市。
参考资料
1.https://www.who.int/zh/news-room/fact-sheets/detail/obesity-and-overweight
2.华创新药公众号
3.Mody, R., Manjelievskaia, J., Marchlewicz, E. H., Malik, R. E., Zimmerman, N. M., Irwin, D. E., & Yu, M. (2022). Greater Adherence and Persistence with Injectable Dulaglutide Compared with Injectable Semaglutide at 1-Year Follow-up: Data from US Clinical Practice. Clinical therapeutics, 44(4), 537–554. https://doi.org/10.1016/j.clinthera.2022.01.017
4.Venniyoor A. (2022). Tirzepatide Once Weekly for the Treatment of Obesity. The New England journal of medicine, 387(15), 1433–1434. https://doi.org/10.1056/NEJMc2211120
5.Wilding, J. P. H., Batterham, R. L., Davies, M., Van Gaal, L. F., Kandler, K., Konakli, K., Lingvay, I., McGowan, B. M., Oral, T. K., Rosenstock, J., Wadden, T. A., Wharton, S., Yokote, K., Kushner, R. F., & STEP 1 Study Group (2022). Weight regain and cardiometabolic effects after withdrawal of semaglutide: The STEP 1 trial extension. Diabetes, obesity & metabolism, 24(8), 1553–1564. https://doi.org/10.1111/dom.1472
6.https://clinicaltrials.gov/study/NCT05422378
7.圣诺官网
8.Deaton, A. M., Dubey, A., Ward, L. D., Dornbos, P., Flannick, J., AMP-T2D-GENES Consortium, Yee, E., Ticau, S., Noetzli, L., Parker, M. M., Hoffing, R. A., Willis, C., Plekan, M. E., Holleman, A. M., Hinkle, G., Fitzgerald, K., Vaishnaw, A. K., & Nioi, P. (2022). Rare loss of function variants in the hepatokine gene INHBE protect from abdominal obesity. Nature communications, 13(1), 4319. https://doi.org/10.1038/s41467-022-31757-8
9.Alnylam官网
10.Wave官网
11.Akbari, P., Gilani, A., Sosina, O., Kosmicki, J. A., Khrimian, L., Fang, Y. Y., Persaud, T., Garcia, V., Sun, D., Li, A., Mbatchou, J., Locke, A. E., Benner, C., Verweij, N., Lin, N., Hossain, S., Agostinucci, K., Pascale, J. V., Dirice, E., Dunn, M., … Lotta, L. A. (2021). Sequencing of 640,000 exomes identifies GPR75 variants associated with protection from obesity. Science (New York, N.Y.), 373(6550), eabf8683. https://doi.org/10.1126/science.abf868
12.Li Y, Zhu G (2023) Ketohexokinase (KHK) Physiology and Treatments in Obesity and Fructose Metabolism. J Obes Weight Loss Ther S6:002.
13.Altamira Therapeutics官网
14.OliX Pharmaceuticals官网
15.Bullfrogai官网
16.10XBIO

 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏

用户评论
这个标题听着就很有科技感!期待看到这篇文章能详细介绍siRNA技术应用于减肥研究的情况,希望能早日看到效果显着的减肥药。
有8位网友表示赞同!
我一直很关注新的减肥方法,siRNA听起来像是挺新颖的。文章里最好能解释一下它到底是怎么工作的原理,以及有什么潜力和局限性?
有9位网友表示赞同!
减肥一直是困扰很多人的问题,希望能有更安全高效的方法,siRNA药剂或许就是我们期待的突破吧!不过,还需要更多科学研究证实它的有效性和安全性。
有10位网友表示赞同!
虽然听起来很有科技感,但我还是比较担心这种新式的药物会有哪些副作用。希望后续文章能详细讨论这个问题,权衡利弊再决定是否尝试使用。
有9位网友表示赞同!
siRNA减肥药的发展方向挺好,但现在很多减肥产品宣称效果显著却实际上没什么用,让人很难相信!希望能看到更多客观可靠的数据支持siRNA的疗效。
有11位网友表示赞同!
我对这种新技术很有兴趣,但是我也想了解一下它的研发难度有多大? 毕竟从实验室研究到临床应用需要很长时间和大量的资金投入,希望它能够顺利推进,早日惠及大众。这篇文章会不会介绍一些相关的公司和机构呢?
有9位网友表示赞同!
其实我觉得减肥的重点还是在于改变生活方式,运动和饮食控制才是长久之计。虽然siRNA药剂或许是一个辅助手段,但更重要的是要养成健康的习惯。
有7位网友表示赞同!
我曾经试过很多种减肥方法,效果都不理想,现在看到siRNA这个新技术,是不是终于看到了曙光?希望这篇文章能详细介绍一下它的使用过程和注意事项,让我能够更好地了解它!
有20位网友表示赞同!
我觉得这种科技发展方向很有前景! 如果能控制好脂肪的生成,就可以有效解决肥胖问题了。 这篇博文写得挺好的,希望能有更多的人关注这种新技术的发展方向。
有19位网友表示赞同!
siRNA减肥药真的太棒了!终于不再需要忍受那些无效果和副作用强大的减肥产品折磨了! 期待后续的文章能介绍一下它的市场前景?
有8位网友表示赞同!
从文章中了解到,siRNA技术还有很多待解决的问题,比如潜在的副作用和靶向特异性。希望后续的研究能够更加深入全面,确保这种减肥药的安全性和有效性。
有6位网友表示赞同!
这篇博文真是太赞了!对最新的siRNA技术进展有了更清晰的认识,现在科技发展的速度真是越来越快了。希望能看到更多关于siRNA技术的应用领域。
有7位网友表示赞同!
我觉得标题有点吓人,我可不想为了减肥试这种新药啊! 希望它能安全可靠,别有什么意外副作用出来弄得人心惶惶!
有8位网友表示赞同!
这个标题太吸引人了,我已经迫不及待想知道siRNA减肥药究竟是如何工作的?有没有什么临床研究成果可以参考?
有12位网友表示赞同!
我不太懂siRNA技术,文章里能不能用通俗易懂的语言解释一下它的主要原理?还有就是它应用于减肥有哪些具体的优势和劣势?
有20位网友表示赞同!
这种新技术听起来挺吓人的吧! 我更倾向于通过运动和饮食控制来减肥,感觉自然健康一点。 希望siRNA药剂不要给人们带来副作用或者其他未知风险。
有12位网友表示赞同!
我觉得这篇博文写的很好,能让我对siRNA技术有更深入的了解。 作为研究人员,应该不断更新科技知识,并鼓励更多人关注科学领域的发展。
有15位网友表示赞同!
siRNA减肥药前景不错,但不能盲目追求快速的减肥效果,还是要注重健康安全的原则,理性看待新的减肥方式。
有10位网友表示赞同!